无法提供相关原始记录样本无法溯源样本重复使用提交的注册报告与临床机构保存的报告不一致签章不一致临床试验未严格按临床方案操作未真实记录不良反应临床试验方案版本不一致、患者按照不同的方案执行受试者无就诊记录,无法核实受试者参加临床试验的真实性
一般,同一个项目在不同临床试验机构被检查出的问题基本是一致的,这其实是申办者对于临床试验态度的问题,而不是偶然因素。现在对于医疗器械的监管越来越严格,抱有侥幸心理,企图蒙混过关终是要付出代价的。
下表是在临床试验实际操作中的常见问题,显然试验方案的合理性是最令人头疼的,还有试验的记录、资料保存等,这些问题也是临床真实性核查中最常见的问题。
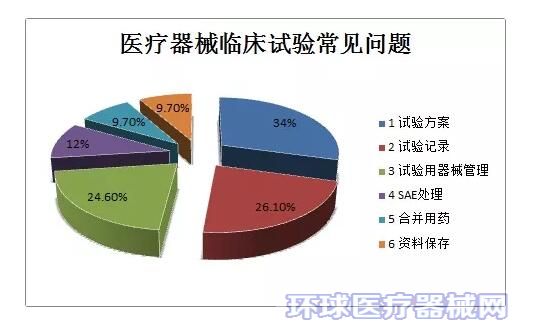
(一) 临床试验方案与临床试验报告问题举例:
1.样本量及各参数的确定没有相关依据:
i. 未提供样本量的具体计算过程及确定依据。
ii. 未提供样本量计算公式中各参数的确定依据,如:非劣效界值。
iii. 未提供临床随访时间的确定依据。
iv. 未明确主要评价指标、次要评价指标及其相关依据。
v. 未明确主要终点指标及时间窗的选择依据。
2.临床资料方案和临床试验报告中内容不对应。临床试验报告应与临床试验方案保持一致,尤其注意明确以下内容:试验产品的产品名称、型号、规格及所对应的试验病种和各个病种的病例数、各病例的随访时间;试验产品的临床适用范围/适应症、禁忌症与注意事项。
3.临床试验主要终点仅考虑即刻的手术成功率,未考虑产品中远期有效性,如:主动脉覆膜支架进行主动脉腔内治疗,临床最为关注的问题是产品的中远期疗效。
4.方案修改后未经伦理委员会审核、样本储存时间和临床试验方案要求不符。在2016年湖北省食品药品监督管理局对医疗器械临床试验进行监督检查时,发现部分申请人存在此类问题。
(二) 试验用器械管理问题举例:
1.试验用医疗器械在临床试验机构使用时应保证在有效期内
2.试验用医疗器械无运输、储存记录或记录不完整。
(三) 临床试验操作中的问题:
临床试验操作中出现的问题基本就是文章开头总结的真实性核查未能通过的企业的常见问题。可见,临床试验的实际操作一定要严格按照方案、法规的要求。试验过程的真实严谨直接关系到临床试验的有效性、真实性。
转自于-----环球医疗器械网


